உள்ளடக்கம்
புரோட்டான்கள், நியூட்ரான்கள் மற்றும் எலக்ட்ரான்கள் ஒரு அணுவை உருவாக்கும் மூன்று முக்கிய துகள்கள். அவர்களின் பெயர்கள் குறிப்பிடுவது போல, முந்தையவை நேர்மறையாக விதிக்கப்படுகின்றன, பிந்தையவர்களுக்கு கட்டணம் இல்லை (அவை நடுநிலையானவை) மற்றும் மூன்றாவது எதிர்மறை கட்டணம். எலக்ட்ரான்கள் மிகக் குறைந்த வெகுஜனத்தைக் கொண்டிருக்கின்றன, அதே நேரத்தில் புரோட்டான்கள் மற்றும் நியூட்ரான்கள் கிட்டத்தட்ட ஒரே மாதிரியான வெகுஜனங்களைக் கொண்டுள்ளன. கால அட்டவணையில் இருந்து தகவல்களை மட்டுமே பயன்படுத்தி அவை ஒவ்வொன்றின் எண்ணிக்கையையும் ஒரு அணுவில் காணலாம்.
படிகள்
2 இன் பகுதி 1: புரோட்டான்கள், எலக்ட்ரான்கள் மற்றும் நியூட்ரான்களைக் கணக்கிடுகிறது
ஒரு கால அட்டவணையைப் பெறுங்கள். இது அணு அமைப்பால் உறுப்புகளை ஒழுங்கமைக்கும் படம். இது வண்ணங்களால் வகைப்படுத்தப்படுகிறது மற்றும் ஒவ்வொரு உறுப்புக்கும் ஒன்று, இரண்டு அல்லது மூன்று எழுத்துக்களின் தனித்துவமான சுருக்கத்தை அளிக்கிறது. பிற தகவல்களில் அணு நிறை மற்றும் எண் ஆகியவை அடங்கும்.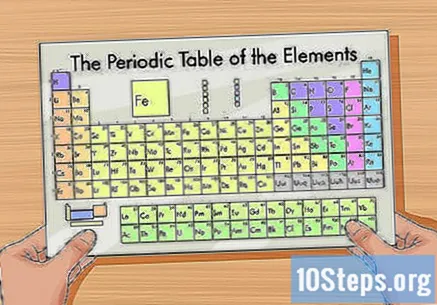
- நீங்கள் ஒரு கால அட்டவணையை ஆன்லைனில் அல்லது வேதியியல் புத்தகத்தில் காணலாம்.
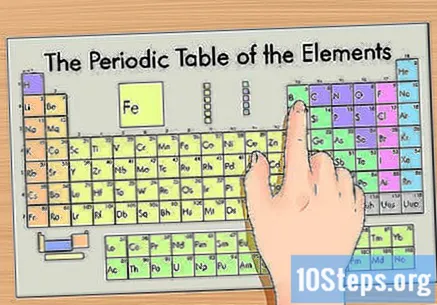
கால அட்டவணையில் உங்கள் உறுப்பைக் கண்டறியவும். இது அணு எண்ணிக்கையால் உறுப்புகளை ஒழுங்குபடுத்துகிறது மற்றும் அவற்றை மூன்று முக்கிய குழுக்களாக பிரிக்கிறது: உலோகங்கள், உலோகங்கள் அல்லாத மற்றும் மெட்டல்லாய்டுகள் (அரை உலோகங்கள்). மற்ற குழுக்களில் கார உலோகங்கள், ஆலசன் மற்றும் உன்னத வாயுக்கள் அடங்கும்.- குழு (நெடுவரிசைகள்) அல்லது காலம் (வரிசைகள்) ஆகியவற்றைப் பயன்படுத்துவது அட்டவணையில் உறுப்பைக் கண்டுபிடிப்பதை எளிதாக்கும்.
- வேறு எந்த பண்புகளும் உங்களுக்குத் தெரியாவிட்டால், உறுப்பு சின்னத்தையும் நீங்கள் தேடலாம்.
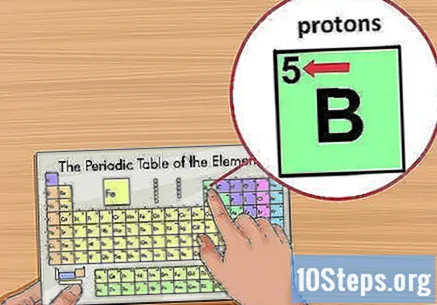
அணு எண்ணைக் கண்டறியவும். இது உறுப்பு சின்னத்திற்கு மேலே, சதுரத்தின் மேல் இடது மூலையில் அமைந்துள்ளது. அந்த உறுப்பின் ஒற்றை அணுவை எத்தனை புரோட்டான்கள் உருவாக்குகின்றன என்பதை அணு எண் உங்களுக்குக் கூறும்.- எடுத்துக்காட்டாக, போரான் (பி) ஒரு அணு எண் 5 ஐக் கொண்டுள்ளது, எனவே ஐந்து புரோட்டான்கள் உள்ளன.
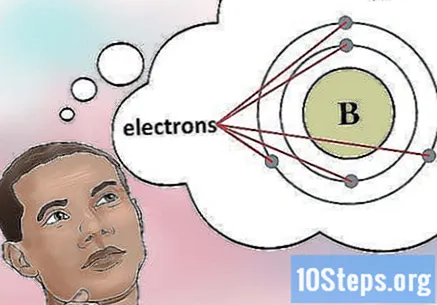
எலக்ட்ரான்களின் எண்ணிக்கையை தீர்மானிக்கவும். புரோட்டான்கள் ஒரு நேர்மறையான கட்டணம் கொண்ட ஒரு அணுவின் கருவில் உள்ள துகள்கள். எலக்ட்ரான்கள் எதிர்மறையாக சார்ஜ் செய்யப்பட்ட துகள்கள். எனவே, ஒரு நடுநிலை உறுப்பு ஒரே எண்ணிக்கையிலான புரோட்டான்கள் மற்றும் எலக்ட்ரான்களைக் கொண்டிருக்கும்.- எடுத்துக்காட்டாக, போரான் (பி) ஒரு அணு எண் 5 ஐக் கொண்டுள்ளது, எனவே ஐந்து புரோட்டான்கள் மற்றும் ஐந்து எலக்ட்ரான்கள் உள்ளன.
- இருப்பினும், உறுப்பு நேர்மறை அல்லது எதிர்மறை அயனியைக் கொண்டிருந்தால், புரோட்டான்கள் மற்றும் எலக்ட்ரான்கள் ஒரே மாதிரியாக இருக்காது. அவற்றை நீங்கள் கணக்கிட வேண்டும். உறுப்புக்குப் பிறகு அயன் எண் சிறிய சூப்பர்ஸ்கிரிப்டாக தோன்றும்.
அணு வெகுஜனத்தைப் பாருங்கள். நியூட்ரான்களின் எண்ணிக்கையைக் கண்டுபிடிக்க, நீங்கள் முதலில் அணு வெகுஜனத்தைக் கண்டுபிடிக்க வேண்டும். இந்த மதிப்பு ஒரு தனிமத்தின் அணுக்களின் சராசரி நிறை மற்றும் உறுப்பு சின்னத்திற்கு கீழே காணலாம்.
- அணு வெகுஜனத்தை அடுத்த முழு எண்ணுக்கு வட்டமிடுங்கள். எடுத்துக்காட்டாக, போரனின் அணு நிறை 10.811 ஆகும், ஆனால் நீங்கள் அதை 11 வரை சுற்றலாம்.
அணு வெகுஜனத்திலிருந்து அணு எண்ணைக் கழிக்கவும். நியூட்ரான்களின் எண்ணிக்கையைக் கண்டுபிடிக்க, நீங்கள் அணு எண்ணை வெகுஜனத்திலிருந்து கழிக்க வேண்டும். அணு எண் புரோட்டான்களுக்கு சமம் என்பதை நினைவில் கொள்ளுங்கள், இது ஏற்கனவே அடையாளம் காணப்பட்டுள்ளது.
- எங்கள் போரான் எடுத்துக்காட்டுக்கு, 11 (அணு நிறை) - 5 (அணு எண்) = 6 நியூட்ரான்கள்
பகுதி 2 இன் 2: அயனிகளைக் கொண்ட எலக்ட்ரான்களைக் கணக்கிடுகிறது
அயனிகளின் எண்ணிக்கையை அடையாளம் காணவும். உறுப்புக்குப் பிறகு இது ஒரு சிறிய சூப்பர்ஸ்கிரிப்ட் மதிப்பாகத் தோன்றும். அயனி என்பது எலக்ட்ரான்களைச் சேர்ப்பது அல்லது அகற்றுவதால் நேர்மறை அல்லது எதிர்மறை கட்டணம் கொண்ட அணு ஆகும். ஒரு அயனியில், புரோட்டான்களின் எண்ணிக்கை அப்படியே இருந்தாலும், எலக்ட்ரான்களின் எண்ணிக்கை மாறுகிறது.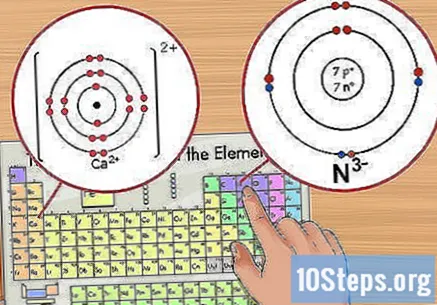
- எலக்ட்ரானுக்கு எதிர்மறை கட்டணம் இருப்பதால், அது அகற்றப்படும்போது, அயனி நேர்மறையாகிறது. அதிக எலக்ட்ரான்கள் சேர்க்கப்படுவதால், அயன் எதிர்மறையாகிறது.
- எடுத்துக்காட்டாக, N க்கு -3 கட்டணம் உள்ளது, Ca க்கு +2 கட்டணம் உள்ளது.
- உறுப்புக்குப் பிறகு சூப்பர்ஸ்கிரிப்ட் எண் இல்லை என்றால் இந்த கணக்கீட்டை நீங்கள் செய்யத் தேவையில்லை என்பதை நினைவில் கொள்ளுங்கள்.
அணு எண்ணிலிருந்து கட்டணத்தைக் கழிக்கவும். ஒரு அயனிக்கு நேர்மறை கட்டணம் இருக்கும்போது, அணு எலக்ட்ரான்களை இழந்துள்ளது. அவற்றில் மீதமுள்ள தொகையை கணக்கிட, அணு எண்ணிலிருந்து கூடுதல் கட்டணம் வசூலிக்கவும். நேர்மறை அயனியின் விஷயத்தில், எலக்ட்ரான்களை விட அதிக புரோட்டான்கள் உள்ளன.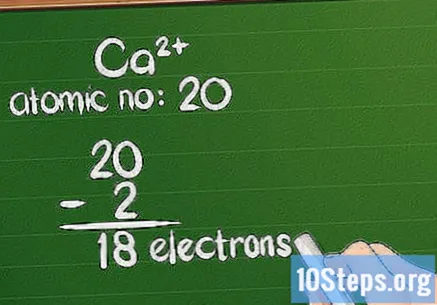
- எடுத்துக்காட்டாக, Ca க்கு +2 கட்டணம் உள்ளது, எனவே அதன் இயல்பான நிலையிலிருந்து 2 எலக்ட்ரான்களை இழந்துள்ளது. கால்சியத்தின் அணு எண் 20, எனவே அயனிக்கு 18 எலக்ட்ரான்கள் உள்ளன.
எதிர்மறை அயனிகளுக்கு அணு எண்ணில் கட்டணத்தைச் சேர்க்கவும். ஒரு அயனிக்கு எதிர்மறை கட்டணம் இருக்கும்போது, அணு எலக்ட்ரான்களைப் பெற்றுள்ளது. அவற்றின் மொத்த எண்ணிக்கையைக் கணக்கிட, நீங்கள் கூடுதல் கட்டணத்தின் அளவை அணு எண்ணில் சேர்க்கிறீர்கள். எதிர்மறை அயனியின் விஷயத்தில், எலக்ட்ரான்களை விட குறைவான புரோட்டான்கள் உள்ளன.
- எடுத்துக்காட்டாக, N க்கு -3 கட்டணம் உள்ளது, எனவே அதன் நடுநிலை நிலையுடன் ஒப்பிடும்போது அது மூன்று எலக்ட்ரான்களைப் பெற்றது. நைட்ரஜனின் அணு எண் 7, எனவே இந்த அயனியில் 10 எலக்ட்ரான்கள் உள்ளன.