உள்ளடக்கம்
பிற பிரிவுகள்ஹைட்ரஜன் மிக இலகுவான உறுப்பு மற்றும் பல தொழில்துறை பயன்பாடுகளைக் கொண்டுள்ளது, இதில் சமையலறையில் பயன்படுத்த ஹைட்ரஜனேற்றப்பட்ட கொழுப்புகளை உருவாக்குதல் மற்றும் நிலக்கரியிலிருந்து ஹைட்ரோகார்பன்கள் உற்பத்தி செய்யப்படுகிறது. இது நீர் மூலக்கூறுகளின் இன்றியமையாத பகுதியாகும், மேலும் சிறிய அளவிலான மின்சாரத்தைப் பயன்படுத்தி பிரிக்கலாம். சில செயலில் உள்ள உலோகங்கள் மற்றும் வலுவான அமிலங்களைப் பயன்படுத்தி ஹைட்ரஜன் வாயுவையும் உருவாக்கலாம். இரண்டு முறைகளும் ஒப்பீட்டளவில் எளிமையானவை மற்றும் ஹைட்ரஜன் வாயுவை சேகரிக்க உங்களை அனுமதிக்கும்.
படிகள்
முறை 1 இன் 2: செயலில் உள்ள உலோகங்களுடன் நீர் இடப்பெயர்ச்சியைப் பயன்படுத்துதல்
தேவையான பொருட்களை சேகரிக்கவும். ஒரு செயலில் உள்ள உலோகத்துடன் ஒரு வலுவான அமிலத்தை கலக்கும் எதிர்வினையைப் பயன்படுத்தி ஹைட்ரஜனை சேகரிக்க, உங்களுக்கு இது தேவைப்படும்: ஒரு எர்லென்மேயர் பிளாஸ்க், ஒரு ரப்பர் ஸ்டாப்பர், பிளாஸ்டிக் குழாய், வடிகட்டிய நீர், சோதனைக் குழாய்கள், ஒரு பெரிய கொள்கலன், 3 மோலார் ஹைட்ரோகுளோரிக் அமிலம் (HCl) மற்றும் மெக்னீசியம் அல்லது துத்தநாகத் துகள்கள்.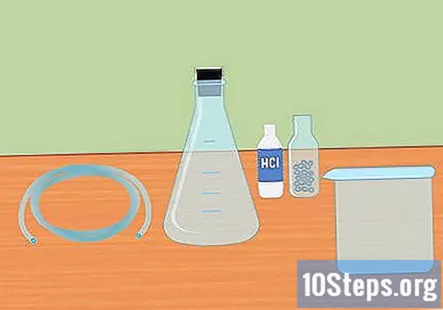
- ஒரு எர்லென்மேயர் குடுவை என்பது ஒரு கண்ணாடி குடுவை ஆகும், இது ஒரு கூம்பு அடி மற்றும் உருளை கழுத்து கொண்டது.
- ரப்பர் தடுப்பவர் பிளாஸ்கின் மேற்பகுதிக்குரியது மற்றும் குழாய்களின் வழியாக செல்ல நடுவில் ஒரு துளை இருக்க வேண்டும்.
- இந்த சோதனைக்கு மெக்னீசியம் அல்லது துத்தநாகம் வேலை செய்யும், உங்களுக்கு இரண்டும் தேவையில்லை.
- இந்த பொருட்களில் சில ஆன்லைனில் அல்லது ஆய்வக விநியோக கடையில் வாங்க வேண்டியிருக்கலாம்.

சரியான பாதுகாப்பு உபகரணங்களை அணியுங்கள். ஹைட்ரோகுளோரிக் அமிலம் போன்ற வலுவான அமிலத்துடன் பணிபுரியும் போது, நீங்கள் சரியான பாதுகாப்பு முன்னெச்சரிக்கை நடவடிக்கைகளை எடுக்கிறீர்கள் என்பதை உறுதிப்படுத்திக் கொள்ள வேண்டும். லேப் கோட் அணிவது, கையுறைகள், மூடிய கால் காலணிகள் மற்றும் கண் பாதுகாப்பு அவசியம்.- கண்ணாடிகள் உங்கள் கண்களின் பக்கங்களைச் சுற்றிக் கொண்டு அவற்றைப் பாதுகாக்க வேண்டும்.
- சரியாக பொருந்தக்கூடிய கையுறைகளை அணியுங்கள், இதனால் உங்கள் கை மற்றும் விரல்களின் நல்ல திறமையை பராமரிக்கலாம்.
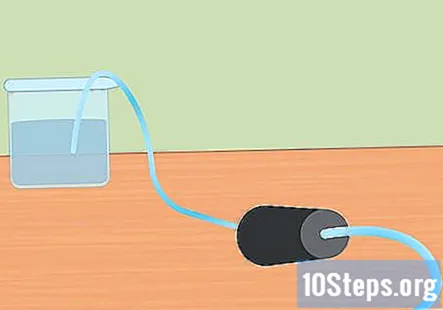
சோதனை அமைப்பைத் தயாரிக்கவும். குழாயின் ஒரு முனையை ரப்பர் தடுப்பவரின் துளைக்குள் செருகவும். குழாய் ரப்பர் தடுப்பான் வழியாக எல்லா வழிகளிலும் சென்று முடிவில் இருந்து சற்று வெளியேற வேண்டும் என்று நீங்கள் விரும்புகிறீர்கள். பெரிய கொள்கலனை தண்ணீரில் நிரப்பி, குழாய்களின் இலவச முடிவை தண்ணீரில் வைக்கவும். சோதனை தொடங்கும் போது, நீங்கள் ரப்பர் ஸ்டாப்பரை எர்லென்மயர் பிளாஸ்கில் வைப்பீர்கள்.- இந்த துண்டுகளை நீங்கள் பயன்படுத்த தயாராக இருக்கும் வரை ஒதுக்கி வைக்கவும்.
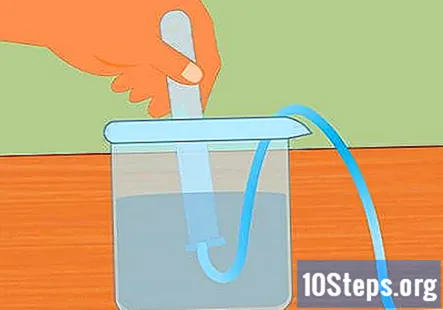
சோதனைக் குழாயை நீரில் மூழ்க வைக்கவும். குறைந்தது ஒரு சோதனைக் குழாயையாவது எடுத்துக் கொள்ளுங்கள் (நீங்கள் அதிக ஹைட்ரஜனை சேகரிக்க விரும்பினால் அதிகமாகப் பயன்படுத்தலாம்) அதை நீரில் மூழ்க வைக்கவும். அனைத்து காற்று குமிழ்கள் தப்பிக்க குழாயை சாய்த்து விடுங்கள். எதிர் முனையில் ரப்பர் தடுப்போடு இணைக்கப்பட்ட நீரில் மூழ்கிய குழாய்களின் மேல் குழாய் வைக்கவும்.- நீங்கள் தொடங்குவதற்கு முன்பு அனைத்து காற்று குமிழ்கள் குழாயிலிருந்து அகற்றப்படுவது அவசியம். அவை இல்லையென்றால், குழாயில் சேகரிக்கப்பட்ட வாயு வெறும் ஹைட்ரஜனை விட அதிகமாக இருக்கும்.
எர்லென்மேயர் பிளாஸ்கில் ஹைட்ரோகுளோரிக் அமிலத்தைச் சேர்க்கவும். பிளாஸ்கை பாதியிலேயே நிரப்ப போதுமான ஹைட்ரோகுளோரிக் அமிலத்தைச் சேர்க்கவும். சுமார் 100 எம்.எல் போதுமானதாக இருக்க வேண்டும். அமிலத்தைச் சேர்ப்பதற்கு முன்பு குடுவை சுத்தமாகவும் உலர்ந்ததாகவும் இருப்பதை உறுதிப்படுத்திக் கொள்ளுங்கள். ரப்பர் கையுறைகளை அணிந்து, குடுவை நிரப்பும்போது எச்சரிக்கையுடன் பயன்படுத்தவும்.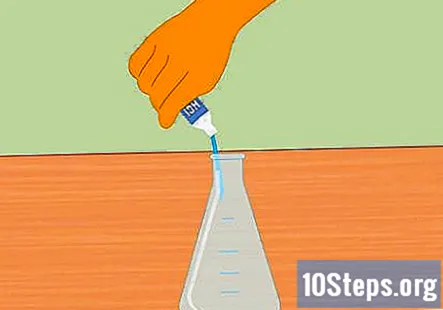
- எந்த நீரையும் அமிலத்தில் கொட்டாமல் பார்த்துக் கொள்ளுங்கள். அமிலத்தில் சேர்க்கப்படும் நீர் வெடிப்பு மற்றும் காயத்திற்கு வழிவகுக்கும்.
எச்.சி.எல் இல் உலோகத் துகள்களைச் சேர்ப்பதன் மூலம் ரசாயன எதிர்வினையைத் தொடங்கவும். பிளாஸ்கில் உள்ள ஹைட்ரோகுளோரிக் அமிலத்தில் ஒரு சில துத்தநாகம் அல்லது மெக்னீசியம் துகள்களைச் சேர்க்கவும். நீங்கள் வைத்த சரியான அளவு முக்கியமல்ல, ஆனால் எதிர்வினையைத் தொடங்க ஒரு சிறிய கைப்பிடி போதுமானதாக இருக்க வேண்டும்.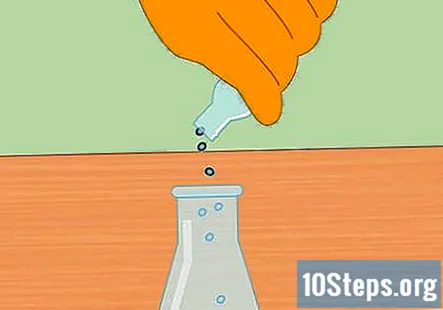
- துகள்களைச் சேர்த்த பிறகு, ஸ்டாப்பரை பிளாஸ்கில் வைக்கவும், இதனால் கணினி இப்போது மூடப்பட்டுள்ளது.
நீரில் மூழ்கிய சோதனைக் குழாயில் ஹைட்ரஜனை சேகரிக்கவும். உலோகம் அமிலத்துடன் வினைபுரியும் போது, ஹைட்ரஜன் வாயு உற்பத்தி செய்யப்படுகிறது. இந்த ஹைட்ரஜன் பிளாஸ்கின் மேற்புறத்திலும், குழாய் வழியாகவும், நீரில் மூழ்கிய சோதனைக் குழாயிலும் பயணிக்கிறது. வாயு தண்ணீரை இடம்பெயரும் மற்றும் சோதனைக் குழாயின் மேற்புறத்தில் ஒரு குமிழி வடிவத்தைக் காண வேண்டும்.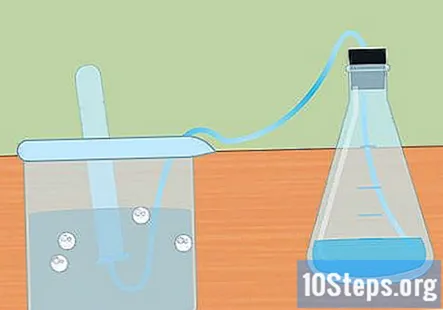
- சோதனைக் குழாய் ஹைட்ரஜனை நிரப்பும்போது, மற்றொரு குழாயை தண்ணீரில் மூழ்கடித்து குழாய் மீது வைக்கவும். உங்கள் எதிர்வினையால் உற்பத்தி செய்யப்படும் அளவுக்கு ஹைட்ரஜனை நீங்கள் சேகரிக்கலாம்.
- ஹைட்ரஜன் வாயு காற்றில் வெளியேறாமல் தடுக்க சோதனைக் குழாய்களை கீழே எதிர்கொள்ளுங்கள்.
வாயு ஹைட்ரஜன் என்பதை உறுதிப்படுத்தவும். வாயு ஹைட்ரஜன் என்பதை உறுதிப்படுத்த, நீங்கள் பிளவு சோதனை என்று அழைக்கப்படுவதை செய்யலாம். ஒரு போட்டியை ஒளிரச் செய்து குழாயின் அடியில் வைத்திருங்கள். ஹைட்ரஜன் இருப்பதைக் குறிக்கும் “பாப்” அல்லது சத்தமிடும் ஒலியை நீங்கள் கேட்பீர்கள்.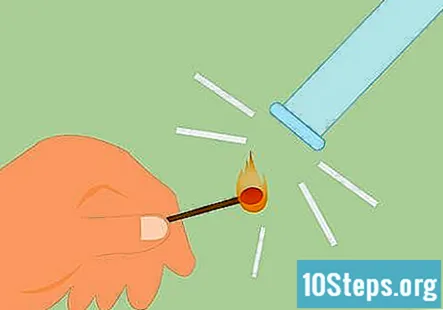
முறை 2 இன் 2: மின்னாற்பகுப்பைப் பயன்படுத்துதல்
தேவையான பொருட்களை சேகரிக்கவும். இந்த சோதனையில், நீரின் மூலக்கூறுகளிலிருந்து ஹைட்ரஜன் மற்றும் ஆக்ஸிஜன் வாயுக்களை பிரிக்க மின்சாரத்தைப் பயன்படுத்துவீர்கள். மின்னாற்பகுப்பைப் பயன்படுத்தி ஹைட்ரஜன் வாயுவைச் சேகரிக்க, உங்களுக்கு 9 வோல்ட் பேட்டரி, ஒரு பென்சில், இரண்டு சோதனைக் குழாய்கள், ஒரு பிளாஸ்டிக் கொள்கலன், நீர், பேக்கிங் சோடா, இரண்டு பெரிய ரப்பர் பேண்டுகள் (விரும்பினால்) மற்றும் இறுதியில் கவ்விகளுடன் கூடிய பேட்டரி கிளிப் தேவைப்படும்.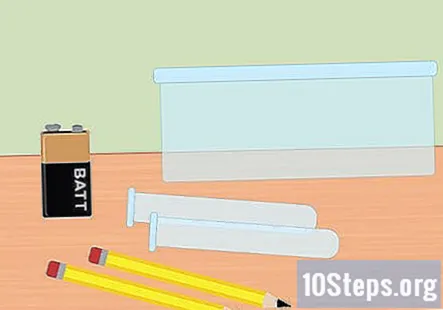
- இது வேலை செய்ய பென்சிலில் கிராஃபைட் இருக்க வேண்டும். ஒரு எண் 2 பென்சில் சரியானது. கிராஃபைட்டின் இரண்டு சிறிய துண்டுகளும் இதற்கு வேலை செய்யும்.
- ஒரு சிறிய உணவு சேமிப்பு கொள்கலன் அல்லது கிண்ணம் போதுமானது.
- பேட்டரி கிளிப் 9 வோல்ட் பேட்டரிக்கு பொருந்தக்கூடியது என்பதையும், இறுதியில் அலிகேட்டர் கவ்விகளுடன் சிவப்பு மற்றும் கருப்பு கம்பி இருப்பதையும் உறுதிப்படுத்திக் கொள்ளுங்கள். இந்த கவ்வியில் உங்கள் கணினியை பேட்டரிக்கு இணைக்க பயன்படும்.
அழிப்பான் பென்சிலிலிருந்து அகற்றி பென்சிலை பாதியாக உடைக்கவும். உங்களுக்கு இரண்டு கிராஃபைட் துண்டுகள் தேவை, ஒன்று பேட்டரியின் நேர்மறையான முடிவு மற்றும் பேட்டரியின் எதிர்மறை முடிவுக்கு. பென்சிலின் ஒவ்வொரு துண்டின் இரு முனைகளையும் ஒரு புள்ளியில் கூர்மைப்படுத்துங்கள். கிராஃபைட் நன்கு வெளிப்படும் என்பதை உறுதிப்படுத்திக் கொள்ளுங்கள்.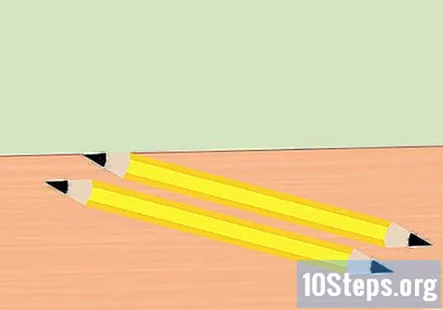
- உங்களிடம் ஏற்கனவே இரண்டு தூய கிராஃபைட் இருந்தால் இந்த படி தவிர்க்கப்படலாம்.
கொள்கலனைச் சுற்றி 2 ரப்பர் பேண்டுகளை எக்ஸ் வடிவத்தில் மடிக்கவும். இந்த படி விருப்பமானது, ஆனால் சோதனை இயங்கும் போது சோதனைக் குழாய்களை வைக்க எளிதான வழியாகும். கொள்கலன் மீது ஒரு ரப்பர் பேண்டை நீட்டி, அதன் மேல் இரண்டாவது ரப்பர் பேண்டை நீட்டவும், இதனால் அது முதல் குறுக்கே சென்று ஒரு எக்ஸ் உருவாகிறது.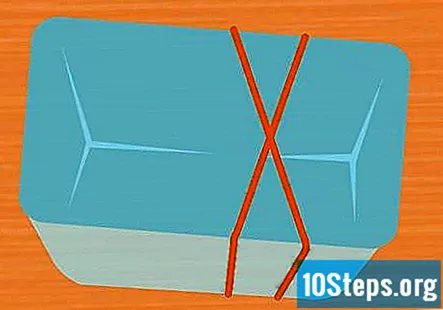
- நீங்கள் ரப்பர் பேண்டுகளைப் பயன்படுத்தாவிட்டால், சோதனைக் குழாய்களை டேப் அல்லது சரம் மூலம் பாதுகாப்பதை உறுதிப்படுத்திக் கொள்ளுங்கள், இதனால் அவை சோதனையின் போது தலைகீழாக இருக்கும்.
ஒரு சமையல் சோடா மற்றும் நீர் கரைசலை உருவாக்கவும். பேக்கிங் சோடாவை நீரில் கரைப்பது மின்சாரத்தை கணினியில் நடத்த உதவும். சேர்க்கப்பட்ட சமையல் சோடாவின் சரியான அளவு முக்கியமல்ல, ஆனால் 1 கப் தண்ணீருக்கு சுமார் 1 டீஸ்பூன் போதுமானதாக இருக்க வேண்டும். முற்றிலும் கரைக்கும் வரை கிளறவும்.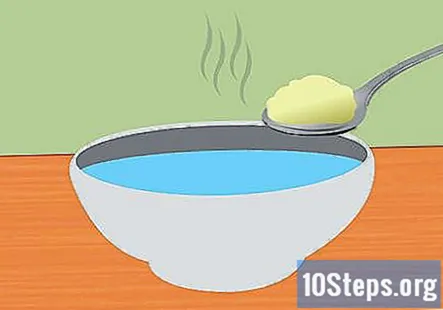
- பேக்கிங் சோடாவைக் கரைப்பதை வேகப்படுத்த வெதுவெதுப்பான நீரைப் பயன்படுத்துங்கள்.
பேக்கிங் சோடா கரைசலில் பிளாஸ்டிக் கொள்கலன் மற்றும் சோதனைக் குழாய்களை நிரப்பவும். சோதனைக் குழாய்கள் இரண்டையும் வைத்திருக்க கொள்கலன் பெரியதாக இருக்க வேண்டும். முக்கால்வாசி நிரப்பப்பட்ட கொள்கலனை நிரப்ப போதுமான தீர்வு சேர்க்கவும். சோதனைக் குழாய்களை கொள்கலனின் கரைசலில் மூழ்கடித்து தலைகீழாக புரட்டவும். ஒவ்வொரு குழாயையும் ரப்பர் பேண்ட் எக்ஸ் சிலுவையில் வைக்கவும்.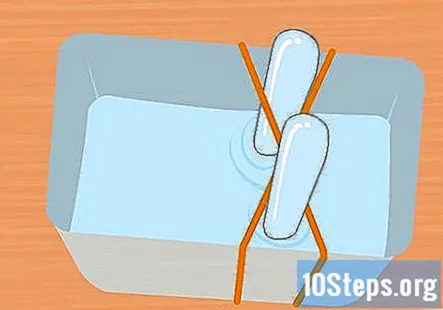
- இரண்டு சோதனைக் குழாய்களும் முற்றிலும் தண்ணீரில் நிரம்பியுள்ளன, காற்று குமிழ்கள் எஞ்சியிருப்பது மிகவும் முக்கியம்.
அலிகேட்டர் கவ்விகளை கிராஃபைட்டுடன் இணைக்கவும். பேட்டரி கிளிப்பிலிருந்து ஒரு கிளம்பை எடுத்து பென்சில்களில் ஒன்றின் இறுதியில் இணைக்கவும். இது முடிந்தவரை கிராஃபைட்டைத் தொடுவதை உறுதிசெய்க. மீதமுள்ள அலிகேட்டர் கிளாம்ப் மற்றும் பென்சில் துண்டுடன் இதைச் செய்யுங்கள்.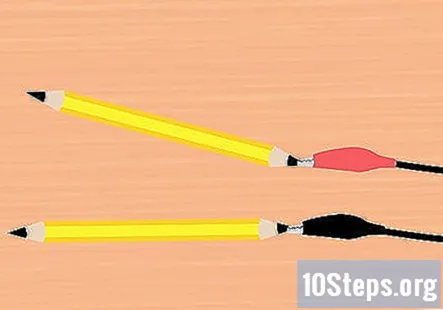
- சிவப்பு கிளம்புடன் ஒரு பென்சிலையும் கருப்பு கிளம்பிற்கு ஒரு பென்சிலையும் இணைக்க வேண்டும்.
சோதனைக் குழாயில் பென்சிலின் அவிழ்க்கப்படாத முடிவை ஸ்லைடு செய்யவும். சோதனைக் குழாயை முழுவதுமாக மூழ்கடித்து, சிறிது சாய்த்து, அதனால் பென்சிலின் கட்டப்படாத முடிவை குழாயில் சறுக்கி விடலாம். இந்த செயல்முறையை மற்ற பென்சில் மற்றும் பிற சோதனைக் குழாயுடன் செய்யவும்.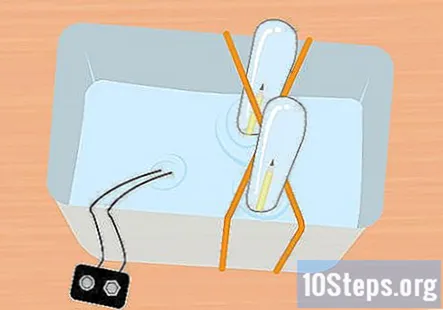
- இந்த கட்டத்தில், எல்லாமே நீருக்கடியில் இருக்க வேண்டும் மற்றும் ஒவ்வொரு சோதனைக் குழாயினுள் ஒரு துண்டு பென்சில் இருக்க வேண்டும்.
- பேட்டரியுடன் இணைக்கும் பேட்டரி கிளிப்பின் முடிவை தண்ணீரிலிருந்து வெளியே வைக்கவும்.
பேட்டரி கிளிப்பை 9 வோல்ட் பேட்டரியுடன் இணைக்கவும். எல்லாம் அமைக்கப்பட்ட நிலையில், இப்போது 9 வோல்ட் பேட்டரி வழங்கிய மின்சாரத்தைப் பயன்படுத்த நீங்கள் தயாராக உள்ளீர்கள். பேட்டரி கிளிப்பின் முடிவானது கொள்கலனில் இருந்து ஒட்டிக்கொண்டிருக்க வேண்டும், எனவே பேட்டரியை அந்த இடத்தில் கிளிப் செய்யுங்கள். பேட்டரி இணைக்கப்பட்டவுடன், கிராஃபைட்டின் முடிவில் இருந்து குமிழ்கள் உயர்ந்து ஒவ்வொரு சோதனைக் குழாயின் மேற்புறத்திலும் மிதப்பதை நீங்கள் கவனிக்க வேண்டும்.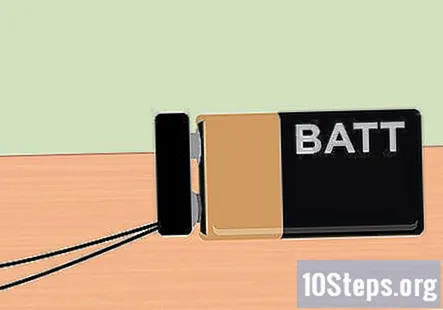
- குமிழ்கள் தயாரிக்கப்படுவதை நீங்கள் காணவில்லை எனில், அலிகேட்டர் கவ்வியில் பென்சிலின் கிராஃபைட்டுடன் உறுதியாக இணைக்கப்பட்டுள்ளதா என்பதை சரிபார்க்கவும். மேலும், உங்கள் பேட்டரி முழுமையாக சார்ஜ் செய்யப்பட்டுள்ளதா என சரிபார்க்கவும்.
- பென்சிலுடன் இணைக்கப்பட்ட எதிர்மறை கம்பி கொண்ட சோதனைக் குழாய் ஹைட்ரஜனை உருவாக்கும், அதே நேரத்தில் பேட்டரியின் நேர்மறை கம்பியுடன் இணைக்கப்பட்ட சோதனைக் குழாய் ஆக்ஸிஜனை உருவாக்கும்.
ஒவ்வொரு குழாயிலும் சில அங்குல வாயு இருக்கும் வரை இரண்டு சோதனைக் குழாய்களில் ஹைட்ரஜன் மற்றும் ஆக்ஸிஜனை சேகரிக்கவும். நினைவில் கொள்ளுங்கள், பேட்டரியின் எதிர்மறை முனையுடன் இணைக்கப்பட்ட குழாய் ஹைட்ரஜனைக் கொண்டிருக்கும் மற்றும் ஆக்சிஜன் நேர்மறை முடிவுடன் இணைக்கப்பட்ட குழாயில் இருக்கும். சோதனைக் குழாய்களை ஜாடியிலிருந்து அகற்றவும், ஒரு நேரத்தில். அவற்றை தலைகீழாக வைத்து தண்ணீர் வெளியேறட்டும். நீங்கள் பார்க்க முடியாவிட்டாலும் குழாய்களில் உள்ள வாயு இருக்கும்.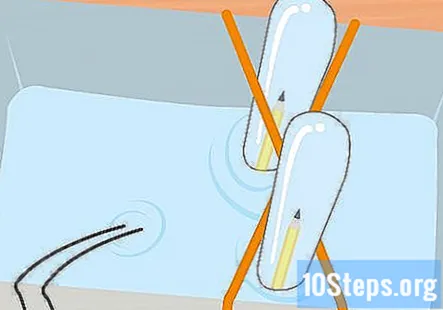
ஹைட்ரஜன் இருப்பதற்கான சோதனை. ஒரு போட்டியைத் தாக்கி, சுடரை வாயு வரை வைத்திருப்பதன் மூலம் ஹைட்ரஜன் இருப்பதை நீங்கள் சோதிக்கலாம். இது ஹைட்ரஜனாக இருந்தால் மிகவும் தனித்துவமான “ஸ்கீக்கி பாப்” ஒலியை உருவாக்கும். போட்டிக்கு பதிலாக லைட் மெழுகுவர்த்தியைப் பயன்படுத்தலாம்.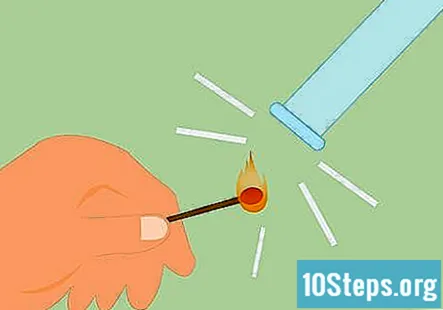
- சக்தி மூலத்தின் நேர்மறையான பக்கத்துடன் இணைக்கப்பட்ட சோதனைக் குழாயில் ஆக்ஸிஜனை சோதிக்க, ஒரு லைட் பொருத்தத்தை (அல்லது மெழுகுவர்த்தியை) ஊதி, சோதனைக் குழாயின் கீழ் இன்னும் ஒளிரும் முடிவை வைக்கவும். மெழுகுவர்த்தி ஆதிக்கம் செலுத்தினால், ஆக்ஸிஜன் உள்ளது.
சமூக கேள்விகள் மற்றும் பதில்கள்
நான் ஹைட்ரஜனை மட்டும் சேகரிக்க விரும்பினால் எனக்கு இரண்டு சோதனைக் குழாய்கள் தேவையா?

சுற்றுச்சூழல் விஞ்ஞானி பெஸ் ரஃப் புளோரிடா மாநில பல்கலைக்கழகத்தில் புவியியல் பி.எச்.டி மாணவர் ஆவார். அவர் 2016 ஆம் ஆண்டில் சாண்டா பார்பராவின் கலிபோர்னியா பல்கலைக்கழகத்தில் சுற்றுச்சூழல் அறிவியல் மற்றும் நிர்வாகத்தில் எம்.ஏ. பெற்றார். கரீபியனில் கடல் சார்ந்த இடஞ்சார்ந்த திட்டமிடல் திட்டங்களுக்கான கணக்கெடுப்புப் பணிகளை நடத்தியுள்ளார் மற்றும் நிலையான மீன்வளக் குழுவின் பட்டதாரி சகாவாக ஆராய்ச்சி ஆதரவை வழங்கியுள்ளார்.

மின்னாற்பகுப்பின் இந்த எளிய பரிசோதனையிலிருந்து எவ்வளவு ஹைட்ரஜனை சேகரிக்க முடியும்? ஹைட்ரஜன் வாயுவின் அழுத்தம் என்னவாக இருக்கும்?
அது சார்ந்துள்ளது. வினையின் வீதம் (நீர் பிரித்தல்) பேட்டரியின் ஆம்ப்ஸ் மற்றும் வினைபுரிய நேரம் ஆகியவற்றை அடிப்படையாகக் கொண்டது. நீங்கள் மிகவும் சூடான அல்லது குளிர்ந்த சூழலில் பரிசோதனை செய்யாவிட்டால் பொதுவாக ஹைட்ரஜன் கடல் மட்ட அழுத்தத்தில் இருக்கும்.
எதிர்மறை குழாயில் ஹைட்ரஜன் ஏன் சேகரிக்கிறது
நீர் மூலக்கூறுகள் எலக்ட்ரான்களைப் பகிர்ந்து கொள்ளும் விதம் காரணமாக, ஹைட்ரஜன் அணுக்கள் நேர்மறையாக சார்ஜ் செய்யப்படுகின்றன மற்றும் ஆக்ஸிஜன் அணுக்கள் எதிர்மறையாக சார்ஜ் செய்யப்படுகின்றன. வாயுக்களை வெளியே எடுக்கும்போது, நேர்மறையாக சார்ஜ் செய்யப்பட்ட ஹைட்ரஜன் எதிர்மறை குழாய்க்கு ஈர்க்கப்படும், அதே நேரத்தில் எதிர்மறையாக சார்ஜ் செய்யப்பட்ட ஆக்ஸிஜன் நேர்மறை குழாயில் ஈர்க்கப்படும்.
எனது எரிவாயு சேகரிக்கும் குழாயிலிருந்து எரிவாயு ஏன் தப்பவில்லை?
இது ஹைட்ரஜன், ஹீலியம் உட்பட மற்ற அனைத்தையும் விட இலகுவானது, அதாவது குழாயின் மூடிய முனை மேலே இருக்கும் வரை இது சோதனைக் குழாயில் இருக்கும், ஏனென்றால் மற்ற வாயுக்கள் அதை இடமாற்றம் செய்கின்றன. ஹைட்ரஜனுக்கு பதிலாக ஹீலியத்தைப் பயன்படுத்துவதற்கான காரணம், அது எரியக்கூடியதல்ல. இது ஒரு உன்னத வாயு (இது 8 எலக்ட்ரான்களின் முழு வேலன்ஸ் ஷெல்லைக் கொண்டுள்ளது) மற்றும் எனவே வினைபுரியாதது என்பதே இதற்குக் காரணம்.
வாயு மிகவும் எரியக்கூடியதாக இருக்குமா?
ஆம். யூடியூப்பில் ஹிண்டன்பர்க் பேரழிவைப் பாருங்கள். செப்பெலின்கள் ஹைட்ரஜனைப் பயன்படுத்தின, ஏனெனில் இது லேசான வாயு, மற்றும் பெற மிகவும் எளிதானது. அதனால்தான் சில கார் தயாரிப்பாளர்கள் ஹைட்ரஜன் இயங்கும் கார்களில் வேலை செய்கிறார்கள்.
இது ஹைட்ரஜனின் திரவ வடிவமா?
இல்லை - இந்த சோதனையில் உள்ள ஹைட்ரஜன் வாயுவாக இருக்கும்
ஹைட்ரஜனை எவ்வாறு திரவமாக்குவது? பதில்
எச்சரிக்கைகள்
- தூய ஹைட்ரஜனுடன் கவனமாக இருங்கள். காற்றில் கலக்கும்போது இது மிகவும் வெடிக்கும்.
- நீங்கள் ஹைட்ரஜனை சேகரிக்கும் சாதனங்களிலிருந்து மற்ற அனைத்து காற்றும் அகற்றப்பட்டுள்ளன என்பதை உறுதிப்படுத்திக் கொள்ளுங்கள்.